线粒体是细胞内最重要的细胞器之一,而细胞内存在多种线粒体质量控制的机制,从而维持细胞内线粒体的稳态。线粒体损伤较小时可以通过线粒体融合、线粒体外膜出泡(MDV)等方式改善线粒体状态。而线粒体自噬以及线粒体蛋白酶降解途径,主要是用来清理细胞内损伤严重的线粒体。而受损严重的线粒体如果不能被及时清理,则会释放大量的死亡因子,从而影响周围健康线粒体的稳态维持,并可能诱导细胞凋亡。
2021年5月27日,澳门尼斯人娱乐网站(中国)有限公司俞立教授实验室在Cell上发表了题为“线粒体分泌,一种迁移体介导的线粒体质量控制机制 (Mitocytosis, a migrasome mediated mitochondrial quality control process)”的研究论文。该论文报道了一种全新的线粒体质量控制机制——线粒体分泌(Mitocytosis),其参与调控细胞内线粒体的稳态维持。这项工作也第一次揭示了迁移体(migrasome)的细胞自主性的功能。
在本研究中,研究者通过电镜观察发现迁移体内存在线粒体,且这些线粒体明显异常于细胞内正常的线粒体,而在正常培养条件下,其迁移体内的线粒体并不太多。研究者尝试在线粒体刺激下,是否会有更多的线粒体进入迁移体内,结果发现:线粒体刺激以及细胞饥饿都可以明显增加迁移体内的线粒体的数量。研究者将细胞通过迁移体将线粒体释放出去的这一现象命名为Mitocytosis,把包含有线粒体的迁移体命名为Mitosome。研究者发现KIF5B、Myosin19及Drp1通过调控线粒体的运输、定位及分裂,从而介导线粒体的分泌,而Dynein的敲低也可以诱导线粒体进入迁移体内。研究者发现在外界刺激下,进入迁移体内的线粒体大部分是受损的,受损线粒体进入迁移体的机制是,受损线粒体与KIF5B结合增强而与Dynein的结合变弱,受损的线粒体更容易被KIF5B运输到细胞边缘而进入迁移体。研究者通过对线粒体的膜电位及呼吸水平的研究,发现Mitocytosis可以维持细胞内的线粒体稳态,因此Mitocytosis可以作为线粒体质量控制的新方式。为了研究Mitocytosis的生理意义,研究者使用小鼠活体观察,发现中性粒细胞在血管中迁移时会产生大量迁移体,并且也伴随着Mitocytosis发生。Mitocytosis通过调控中性粒细胞的线粒体稳态,从而影响循环中性粒细胞在血管中的存活。
澳门尼斯人娱乐网站(中国)有限公司俞立教授为该论文的通讯作者。2016级博士焦海峰与博士后姜东为该论文的共同第一作者。澳门尼斯人娱乐网站(中国)有限公司胡晓瑜、杜万青、李晓鹏、钟丘实、王暄、李英、张静和常在,公司医学院胡小玉教授及其实验室吉亮亮、杨宇卓,北京大学博士研究生彭冰,汪春晖和博士后翁健莉对本文有重要贡献。
俞立教授的研究方向是细胞生物学,自实验室成立以来,一直从事自噬领域的研究,最近,实验室发现了新的细胞器迁移体,目前对其分子机制与生理功能进行深入的研究。细胞自噬领域的研究曾入选2012年中国科学十大进展,俞立教授也于2013年获谈家桢生命科学创新奖,2021年获得中国细胞生物学学会杰出成就奖。
该研究受到国家自然科学基金(基金号:92054301、31790401、32030023),北京市科学技术委员会基金(基金号:Z201100005320019),中国科学技术部基金(基金号:2017YFA0503404 、2016YFA0500202)等资助。
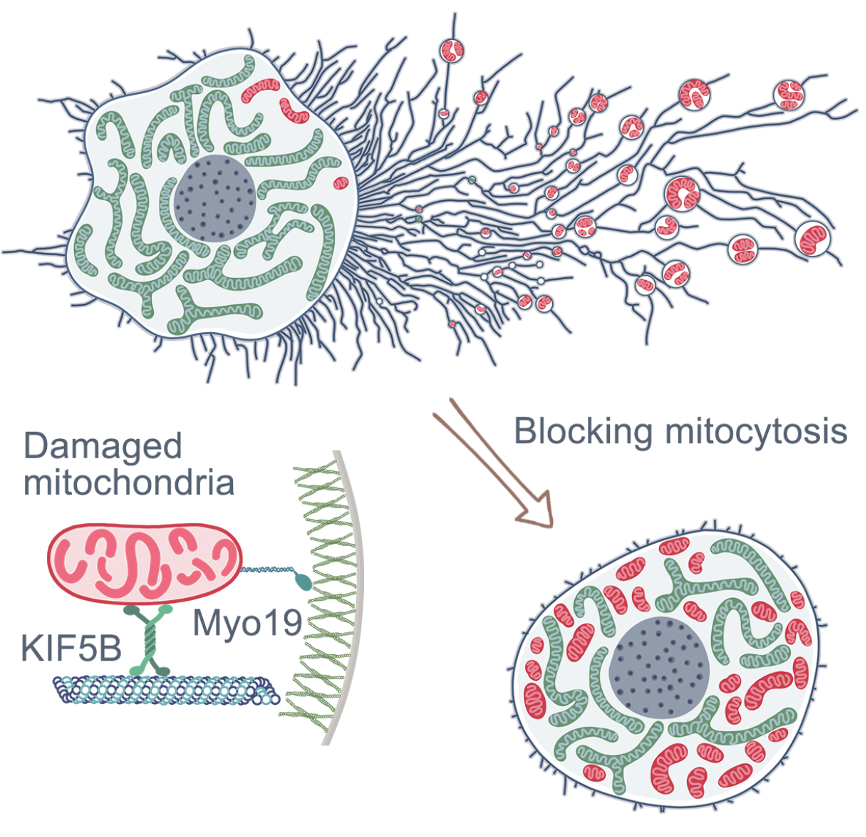
细胞通过迁移体将受损线粒体清理出去,从而维持细胞内线粒体的稳态
原文链接:https://doi.org/10.1016/j.cell.2021.04.027