2021年09月24日,公司葛亮课题组在《细胞研究》(Cell Research)期刊在线发表了题为“TMED9和SEC12蛋白相互作用介导ERGIC-ERES新型内膜互作调节自噬体膜形成”(A new type of ERGIC-ERES membrane contact mediated by TMED9 and SEC12 is required for autophagosome biogenesis)的研究论文,报道了一条由TMED9和SEC12蛋白相互作用介导的ERGIC-ERES新型内膜互作调节自噬体膜形成的分子通路。
细胞自噬是一种由溶酶体介导的细胞内降解途径,在进化上非常保守,其生物学功能涉及诸多方面,与生物的生长发育、衰老、以及人类重大疾病等密切相关。细胞自噬的一个核心步骤是双层膜自噬体的形成,该过程需要内膜系统提供膜来源,并通过内膜形变的方式产生自噬体膜前体。内膜系统是如何转变成自噬体的是自噬领域多年来的谜题之一。
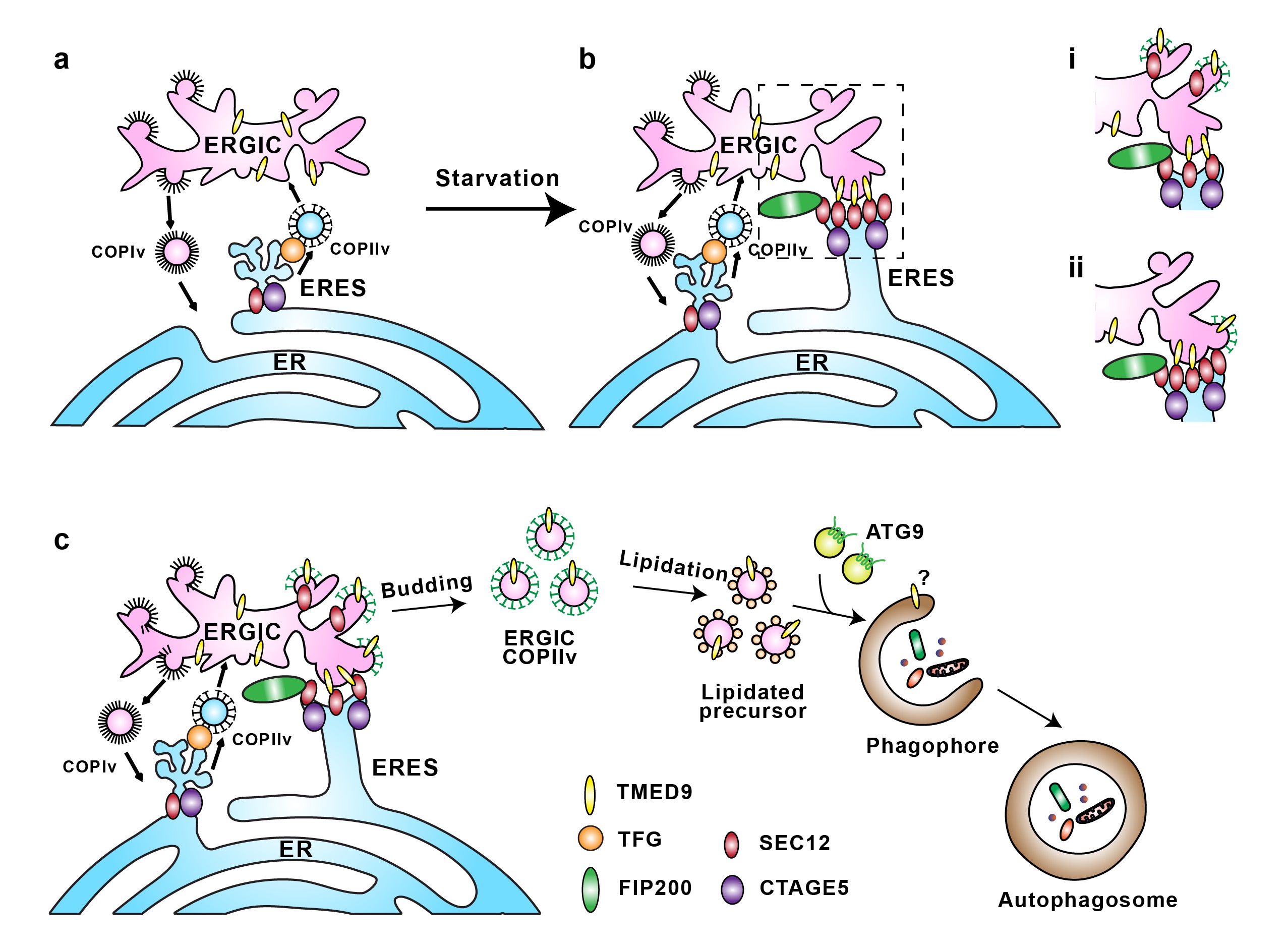
图1. TMED9调节新型内膜ERGIC-ERES互作促进自噬体形成的工作模型
在这项研究中,研究人员通过体外重建自噬体的脂化系统、膜泡分离和质谱鉴定,发现ERGIC蛋白TMED9在调控自噬体产生过程中发挥重要的作用。TMED9缺失细胞内自噬体产生水平下降。先前研究发现饥饿条件下ERES产生形变并和ERGIC 发生联系,该过程调节自噬(Ge et al., 2017)。进一步的研究发现ERGIC上的TMED9通过结合ERES上的SEC12,促使一类新型内膜互作ERGIC-ERES互作的形成。活细胞成像实验发现,ERGIC-ERES互作时间(20-30s)较传统膜互作更短。电子断层扫描3D重构结果显示ERGIC-ERES互作面的最短距离可以达到2-5 nm,提示ERGIC-ERES互作有独特的功能。紧接着,作者发现ERES上的SEC12可以通过短距离互作接触到ERGIC膜,实现在ERES上反式催化ERGIC-COPII小泡的形成从而调节自噬体膜的产生。此外,ERGIC-ERES互作也会调节SEC12从ERES到ERGIC的转位顺式催化ERGIC-COPII产生。结合先前的一系列工作,作者提出了一个TMED9介导的ERGIC-ERES新型膜互作促进自噬体形成的分子通路(图1)。其中,饥饿刺激通过影响SEC12与FIP200以及CTAGE5的互作导致ERES重塑。ERES重塑促进TMED9与SEC12的结合,直接介导了ERGIC-ERES膜互作的形成,可以为SEC12从ERES到ERGIC的转移提供便利条件,而且由于接触非常紧密,位于ERES上的SEC12可以直接反式激活ERGIC上COPII的产生。通过以上两种方式,ERGIC可以在饥饿等胁迫条件下产生COPII自噬小泡,为自噬体的形成提供充足膜来源。
澳门尼斯人娱乐网站(中国)有限公司葛亮副教授为通讯作者,实验室2019级澳门尼斯人娱乐网站博士生李树林是文章的第一作者。此研究得到了膜生物学国家重点实验室、国家基金委、科技部、北京自然科学基金委和生命科学联合中心等经费的支持。
原文链接:https://doi.org/10.1038/s41422-021-00563-0